
INFARMED - #EstamosOn
A pandemia, pela sua particularidade, obrigou a que todos nos adaptássemos a uma nova realidade, uma realidade complexa e, neste sentido, as instituições também tiveram que fazer a sua adaptação, nomeadamente, instituições da área da saúde, com responsabilidades particulares no combate à pandemia.
Desde o início da crise pandémica em Portugal, o INFARMED e as restantes autoridades de saúde têm reunido diariamente, e produzindo e divulgando orientações, com o objetivo de informar os cidadãos de forma clara e transparente, e, neste sentido, assinalamos o regresso da INFARMED Newsletter.
Gostaríamos ainda de salientar algumas das atividades que têm sido desenvolvidas pelo INFARMED, de forma a dotar as entidades e os profissionais de saúde, assim com os cidadãos, das ferramentas necessárias nesta altura atípica, tais como:
- A gestão da Reserva Estratégica de Medicamentos, Dispositivos Médicos e Equipamentos de Proteção Individual. Garantir o abastecimento de Medicamentos Dispositivos Médicos e Equipamentos de Proteção Individual no país, em situações emergentes durante a Pandemia COVID-19.;
- Definir com os profissionais de saúde e doentes a forma de garantir sem descontinuidade a dispensa de medicamentos, em particular os do ambulatório hospitalar;
- Estabelecer regras específicas para a produção nacional de dispositivos médicos;
- Desenvolver normas e orientações necessárias ao funcionamento do sistema do medicamento e produtos de saúde, quer autonomamente, quer em conjunto com outras instituições (Direção-Geral da Saúde, INSA, ASAE, IPQ, etc.)
- A DGS, o INFARMED e o INSA elaboraram recentemente uma Circular Informativa Conjunta sobre o tema Testes laboratoriais para SARS-CoV-2, focando também os Testes Rápidos
- Manter um diálogo frequente e regular com todos os parceiros do sistema, Indústria farmacêutica e de dispositivos médicos, Grossistas, Farmácias, Serviços de saúde, Associações Profissionais, Associações de Doentes e Ordens Profissionais.
- Promover a articulação a nível europeu na rede de autoridades.
Mas claro, os desafios continuam. Agora cada vez mais focados nos novos medicamentos e vacinas por que todos ansiamos.
Relembramos ainda que no website do INFARMED pode aceder a todas as informações e diplomas legais relativas à COVID-19 no âmbito da atividade do INFARMED.
Esperamos continuar a contribuir com a divulgação de todas as informações relevantes e atuais.

Visita da Secretária de Estado Adjunta e da Saúde ao INFARMED
Durante o mês de maio, a Secretária de Estado Adjunta e da Saúde, Jamila Madeira realizou uma visita ao INFARMED.
Esta reunião, onde foi feito um balanço da atividade desenvolvida pelo INFARMED no quadro de resposta do Serviço Nacional de Saúde (SNS) à COVID-19, contou ainda com uma visita ao Laboratório de Comprovação da Qualidade.
A função determinante do INFARMED na gestão das reservas estratégicas, no tratamento e utilização de medicamentos experimentais, na verificação e avaliação dos testes de diagnóstico, no enquadramento adequado de doações, na certificação de novos dispositivos médicos, bem como na garantia de abastecimento e acesso ao medicamento pelos portugueses foram alguns dos temas apresentados.
Respeitando as condicionantes impostas pela realidade atual, foi possível a “presença” dos colaboradores do INFARMED, através de teleconferência, para que pudessem assistir à sessão.

Alterações ao Regulamento Interno do INFARMED
Foi publicado no Diário da República n.º 66/2020, Série II de 02-04-2020, a Deliberação n.º 421/2020, do Conselho Diretivo que aprovou alterações ao Regulamento Interno do INFARMED, que visam dar resposta a necessidades operacionais e estratégicas e visam dar resposta aos novos desafios de gestão relativos ao desenvolvimento do sistema de saúde, em particular as necessidades e desafios do Serviço Nacional de Saúde, à vertiginosa evolução de novas e cada vez mais complexas tecnologias, bem como aos desafios no âmbito da ciência regulamentar, aliada ao papel crescente dos cidadãos e á necessidade de promover a sua participação nas atividade do INFARMED.
No âmbito das alterações ao regulamento interno agora realizadas é de assinalar:
A revisão dos princípios gerais de funcionamento.
A previsão da criação de áreas de desenvolvimento organizacional como forma de se assegurar a coordenação de esforços em áreas transversais, multidisciplinares, com impacto na estratégia do INFARMED, onde se inserem as áreas já existentes como o Projeto INCLUIR, Canábis para fins medicinais e o Aconselhamento Regulamentar e Científico, e se criam desde já novas áreas como a Gestão do Risco Organizacional, Transformação Digital, Utilização de Dados de Saúde.
A criação da Unidade de projetos interinstitucionais e para o sistema de saúde, com competências especificas na gestão da disponibilidade do medicamento, no desenvolvimento de ações de informação ou articulação de caráter transversal em resposta a necessidades do Serviço Nacional de Saúde (SNS) e de todo o Sistema de Saúde, e no âmbito dos projetos e iniciativas de caráter interinstitucional, nomeadamente no âmbito do Ministério da Saúde e de outras entidades públicas e privadas.
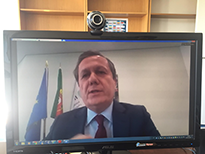
Portugal participa em iniciativa inovadora com OMS e parceiros
Na passada sexta feira (29/maio), através de teleconferência, trinta países e vários parceiros e instituições internacionais participaram no lançamento da iniciativa COVID-19 Technology Access Pool (C-TAP), uma iniciativa destinada a tornar vacinas, testes, tratamentos e outras tecnologias em saúde para combater o COVID-19 acessível a todos.
O encontro foi proposto pela primeira vez em março pelo Presidente Carlos Alvarado, da Costa Rica, que se juntou ao diretor-geral da OMS, Dr. Tedros Adhanom Ghebreyesus e aos restantes subscritores da iniciativa, no lançamento oficial da iniciativa.
A representar Portugal, Rui Santos Ivo, Presidente do INFARMED, enfatizou que “Esta iniciativa exige uma prioridade global no acesso equitativo a produtos de saúde, reforçando a importância de garantir os princípios de sustentabilidade, disponibilidade e acessibilidade de produtos de saúde seguros, eficazes e de qualidade, que, mais do que nunca, são fundamentais para enfrentar a atual pandemia”.

Estado Português e Indústria Farmacêutica assinam Acordo para 2020
No dia 25 de maio, foi concluída a assinatura do Acordo para o ano de 2020 entre o Estado Português, representado pelos Ministros de Estado e das Finanças, de Estado e da Economia e da Saúde, e a Indústria Farmacêutica, por intermédio da APIFARMA – Associação Portuguesa da Indústria Farmacêutica, no qual se releva a importância de manter os pressupostos que têm vindo a vigorar nos últimos anos, designadamente o contributo para a sustentabilidade da despesa na política do medicamento e do Serviço Nacional de Saúde, tanto por via da eficiência na utilização dos recursos, como da consideração de procedimentos excecionais de alocação de recursos em função de situações extraordinárias.
Pretende-se igualmente reforçar, durante o ano de 2020, a garantia do acesso ao medicamento, as condições estruturais favoráveis ao desenvolvimento dos fatores de atratividade para o investimento em Portugal, e ainda a importância de continuar a garantir uma convergência de esforços nas formas de articulação entre o Estado e os agentes do setor da indústria farmacêutica, tendo presente o contexto nacional decorrente da declaração de pandemia decretada pela Organização Mundial de Saúde.

Rede europeia de regulamentação de medicamentos
totalmente mobilizada em luta contra COVID-19
O desenvolvimento e a disponibilidade de medicamentos e vacinas para todos os cidadãos da União Europeia, incluindo aqueles com COVID-19, é a prioridade número um para a rede de Agências reguladoras do medicamento europeias. A Agência Europeia de Medicamentos (EMA), juntamente com os Estados-Membros da UE e a Comissão Europeia, publicaram um plano delineando os princípios de como a rede garantirá que as normas reguladoras de saúde pública e animal, em atividades como a autorização, manutenção e supervisão de medicamentos para uso humano e veterinário, continuarão a ser observadas durante a pandemia da COVID-19.
O plano visa apoiar o funcionamento contínuo da rede como um todo através de uma consistente abordagem para todos os medicamentos, independentemente de serem autorizados a nível europeu ou nacional.
Pode aceder aqui ao comunicado original.
Reunião Virtual dos Chefes das Agências Europeias do Medicamento
No passado dia 28 de maio, realizou-se a reunião dos Chefes das Agências Europeias do Medicamento sob a Presidência da Croácia, que decorreu em ambiente virtual face ao contexto atual de pandemia. A agenda de trabalho centrou-se no acompanhamento da situação e das medidas preconizadas na área do medicamento e dispositivos médicos pelos Estados Membros, Agência Europeia de Medicamentos e Comissão Europeia. Um dos pontos de relevo assumido de forma unânime diz respeito à aprendizagem decorrente da experiência em contexto da pandemia e que resulta no objetivo de manter e reforçar a comunicação e a harmonização de iniciativas pela Rede Europeia do Medicamento em contexto de crise. O Presidente do Conselho Diretivo do INFARMED, em representação de Portugal, relatou as principais medidas para assegurar a atividade da Agência, bem como a disponibilidade e acesso a medicamentos e equipamentos de proteção individual.

Microsite - ‘Dispositivos Médicos e Equipamento de Proteção Individual’
No âmbito do combate ao novo coronavírus, e de forma a garantir como prioridade absoluta a saúde e a segurança dos cidadãos, é necessário promover a disponibilização dos equipamentos de proteção adequados a quem deles necessite.
Desta forma, houve necessidade de criar orientações para as empresas que se mostraram disponíveis a reconverter as suas linhas de produção e a iniciarem o fabrico de alguns dos produtos necessários nesta situação, sem, no entanto, descurar a sua segurança e qualidade.
O desenvolvimento desta prática promove, não só a garantia do acesso aos produtos de saúde necessários, mas também a atividade económica de algumas empresas em território nacional.
Neste contexto foi criado um microsite com informação sobre as Orientações para a colocação no mercado de produtos sem marcação CE por parte de fabricantes nacionais que habitualmente não os produzem, e onde é possível encontrar, entre outras informações, a lista de fornecedores dos diferentes equipamentos necessários para proteção dos cidadãos. Nesta área, é também possível o registo de novas entidades para o efeito.

73ª Assembleia Mundial da Saúde da OMS aprova moção de resposta à COVID-19
A 73.ª Assembleia Mundial da Saúde da Organização Mundial da Saúde (OMS), reunida por teleconferência, aprovou por consenso, no passado dia 19 de maio, uma resolução, promovida pela União Europeia, intitulada “Resposta à COVID-19”.
A resolução aprovada incentiva os Estados-membros a promoverem uma resposta conjunta ao surto pandémico de COVID-19 e procura também realçar o papel da OMS, estimulando um "acesso universal, rápido e equitativo a todos os produtos necessários para a resposta à pandemia" e apelando para que qualquer vacina seja considerada um "bem público global".
Em termos complementares, a resolução incita a OMS a colaborar de forma estreita com as restantes entidades competentes (Organização Mundial da Saúde Animal, Organização das Nações Unidas para a Agricultura e a Alimentação, etc.) para identificar a fonte zoonótica (animal) do vírus e determinar por que via foi introduzido na população humana.
Entre outros aspetos a assinalar nesta resolução, salientamos o pedido feito aos Estados-Membros para fornecerem informação de saúde pública atempada, precisa e suficientemente pormenorizada no que diz respeito à pandemia de COVID-19, conforme se exige nos Regulamentos Internacionais de Saúde.
Por último, é também feito um apelo aos Estados-membros para promoverem um financiamento sustentável à OMS, de forma a garantir que esta organização responda de forma eficaz às necessidades globais de saúde pública e continue a prestar apoio aos Estados-membros com maiores fragilidades, para que estes possam manter em funcionamento os seus sistemas de saúde e os programas de vacinação, saúde mental, saúde materna, infantil e reprodutiva.

Hidroxicloroquina recomendação de suspensão
O INFARMED e a Direção-Geral da Saúde (DGS) decidiram recomendar a suspensão do tratamento com hidroxicloroquina em doentes com COVID-19. Esta decisão está em linha com a resolução da Organização Mundial de Saúde (OMS), na sequência da publicação de dados que questionam a segurança e a eficácia deste medicamento.
Apesar de o INFARMED e a DGS recomendarem a suspensão do tratamento com este medicamento, alerta-se que estas recomendações só dizem respeito ao uso na COVID-19, sendo que os doentes que estavam a ser tratados com hidroxicloroquina para outras patologias, doenças autoimunes como lúpus eritematoso sistémico, artrite reumatoide e malária, para as quais estas moléculas estão aprovadas, não devem interromper o seu tratamento, que nestas situações se mantem seguro, desde que devidamente acompanhado pelo médico assistente.

Legislação
Este segmento da INFARMED Newsletter divulga a seleção das últimas alterações de legislação, relevantes para a atividade do INFARMED, publicadas em Diário da República e Jornal Oficial da União Europeia. De momento a compilação da legislação está disponível no separador ‘Legislação Compilada’ na área COVID-19 no website do INFARMED.


