 |
 |
Ao
INFARMED, Instituto Nacional da Farmácia e do Medicamento, enquanto
Autoridade Regulamentar do Medicamento e dos Produtos de Saúde, compete
prover informação aos profissionais de saúde no âmbito
das suas actividades.
A Infarmedia - Informação aos Profissionais de Saúde
é, pela sua própria natureza, um espaço de diálogo
e uma forma de disponibilizarmos a estes profissionais o acesso ao conhecimento
derivado da nossa actividade, habilitando-os a uma decisão informada
e a um exercício profissional que garanta a salvaguarda da saúde
pública.
Será uma publicação de apenas uma folha, mensal centrando
a sua atenção em tópicos inovadores ou que consideremos
relevantes nos domínios da eficácia, da qualidade, da segurança
e da acessibilidade, servindo de elo de ligação com todos
os profissionais de saúde, e simultaneamente, funcionando como um
instrumento complementar dos outros meios de informação do
INFARMED e das instituições comunitárias, em particular
da Agência Europeia do Medicamento (EMEA). |
| Recomendações
de utilização |
| Medicamentos
>
Paroxetina
mais>> |
| Dispositivos
Médicos > Risco de meningite bacteriana em crianças
com implantes cócleares mais>> |
| Medicamentos
Genéricos Comparticipados* |
| [substâncias
activas novas] mais>> |
| Medicamentos
Genéricos: Evolução da utilização mais>> |
| Informação
sobre Qualidade |
| Comprovação
da Qualidade mais>> |
| Medicamentos
retirados do mercado mais>> |
| Comparticipações
especiais mais>> |
| Medicamentos
comparticipados* |
| [substâncias
activas ou indicações terapêuticas novas] mais>> |
| Novo
escalão de comparticipação 20% mais>> |
| [substâncias
activas ou indicações terapêuticas novas]
mais>> |
| [medicamentos
genéricos]
mais>>
|
| Como
receber a Infarmedia ? mais>> |
| Recomendações
de utilização |
| Medicamentos
>
Paroxetina |
| O
INFARMED alerta os profissionais de saúde para que a Paroxetina não
deverá ser iniciada em doentes com idade inferior a 18 anos,
para o tratamento de doença depressiva major. Os doentes deste grupo
etário que se encontrem já a fazer tratamento com Paroxetina
para a doença depressiva major devem contactar o seu médico
assistente. A interrupção do tratamento com Paroxetina
deverá efectuar-se de uma forma gradual e sob supervisão médica
por forma a minimizar eventuais riscos associados à descontinuação
da terapêutica. |
| Consulte
Medicamentos contendo paroxetina como substância activa disponíveis
no mercado, no Prontuário Terapêutico ou no site
do INFARMED |
| Dispositivos
Médicos > Risco de meningite bacteriana em crianças
com implantes cócleares |
Reforçando
as recomendações prévias, de forma a diminuir o risco
de meningite bacteriana em indivíduos com implantes cóclerares,
o INFARMED recomenda:
· O seguimento das recomendações de vacinação
da DGS;
· A actualização do registo de vacinação
dos candidatos a implante e dos indivíduos com implante cóclear;
· O reconhecimento precoce dos sinais e sintomas de meningite;
· O pronto diagnóstico e tratamento de qualquer infecção
do ouvido médio;
· A profilaxia prévia ao implante cóclear em crianças. |
| Medicamentos
Genéricos Comparticipados* |
| [substâncias
activas novas] |
|
Escalão
B - 80 %
Claritromicina | Claritomicina Prodome 500mg comprimidos revestidos
| 12, 21 e 28 unidades
Felodipina | Felodipina Bexal 5mg comprimidos de libertação
prolongada | 7 e 30 unidades | Felodipina Bexal 10 mg comprimidos de libertação
prolongada | 30 unidades
* Embalagens disponíveis no mercado, conforme informação
do titular de AIM.
|
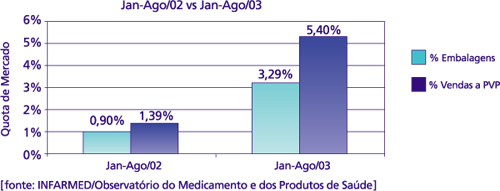
| Medicamentos
Genéricos: Evolução da utilização |
| Informação
sobre Qualidade |
Os
alertas de qualidade são emitidos quando o INFARMED detecta a existência
no mercado de medicamentos com defeitos de qualidade que podem originar
perigo para a Saúde Pública, processando-se de imediato a
retirada do(s) lote(s), do mercado. De acordo com a gravidade dos defeitos
detectados, os alertas são identificados em: Classe I (mais grave),
II, ou III (menos grave).
Os alertas de qualidade podem ter origem nacional ou serem notificados através
das congéneres europeias ou de entidades com as quais Portugal tenha
acordos. O Titular de AIM procede à verificação da
incidência do defeito de qualidade nos lotes recolhidos e investiga
as causas e efeitos relativas à não conformidade detectada.
Medicamentos com defeitos de qualidade minor (classe III ou excepcionalmente
classe II) podem vir a ser reintroduzidos no circuito comercial após
correcção da não conformidade e autorização
do INFARMED. |
| Medicamento |
Defeito
detectado |

| Polio
Sabin® |
|
Defeito
na selagem dos recipientes |

| Ácido
acetilsalicílico Ratiopharm | 500mg comprimidos |
|
Fora das especificações relativamente ao ensaio de dissolução |

| Eprex® |
|
Pequenas
quantidades de substâncias estractíveis provenientes do êmbolo
de borracha, utilizado no processo de fabrico do medicamento |

| Vibrocil®
| solução para inalação por nebulização |
|
Embalagens
cuja formulação não corresponde à
formulação autorizada pelo INFARMED |

| Loride®
| 2mg | comprimidos |
|
Não
cumpre as especificações relativamente ao ensaio de dissolução |

| Istivac®
| suspensão injectável em seringa pré-carregada |
|
Deformação
das agulhas incorporadas em algumas seringas pré-carregadas |

| Consulte
Circulares
informativas para informação detalhada sobre os medicamentos
e lotes recolhidos. |
| Os
resultados do controlo laboratorial, realizado no Laboratório de
Comprovação da Qualidade, a medicamentos e produtos cosméticos
e de higiene corporal são divulgados periodicamente no site do INFARMED,
organizada em listas de acordo com o tipo de produto. |
| Todos
os lotes de vacinas de uso humano distribuídos no mercado nacional,
carecem de aprovação prévia de lote por parte do INFARMED.
A lista dos lotes de vacinas, cujo prazo de validade não caducou,
está disponível no site do INFARMED. |
Consulte
http://infarmed.pt/controlo_laboratorial/
Listas de produtos analisados
Medicamentos (geral) | Medicamentos genéricos |
Medicamentos derivados do plasma humano | Produtos cosméticos e de
higiene corporal |
| Medicamentos
retirados do mercado |
Eficácia
e segurança insuficientemente comprovadas
Diertina® Dihidroergocristina (mesilato) | Solução
oral | 2mg/ml |
| Os
Alertas de Segurança e os Alertas de Qualidade são
enviados aos diversos intervenientes do circuito do medicamentos e dos produtos
de saúde. Podem ainda ser consultados no site do INFARMED em: www.infarmed.pt |
| Comparticipações
especiais |
Os
custos com o fornecimento de medicamentos comparticipados a doentes com
lúpus, hemofilia ou hemoglobinopatias são integralmente
suportados pelo SNS, desde que o prescritor assinale na receita de que se
trata de um doente abrangido pelo Despacho nş 11 387-A/2003 (2Ş série).
[ambulatório]
Esclerose múltipla (EM) | Glatiramero (acetato) | Copaxone®
| pó e solvente para solução injectável | 20mg/1
ml | 28 unidades.
Este medicamento, tal como os anteriormente incluídos (interferão
beta), é comparticipado pelo escalão A (100%), desde que prescrito
por médicos neurologistas, nos respectivos serviços especializados
dos hospitais no SNS, devendo da receita constar referência explícita
ao Despacho nş 19 066/98 (2Ş série).
[hospital] |
| Medicamentos
comparticipados* |
| [substâncias
activas ou indicações terapêuticas novas] |
 |
|
Escalão
B – 70 %
Brometo de tiotrópio | pó para inalação,
cápsula dura | 0,018mg | Spiriva® | 30 unidades | Boehringer
Ingelheim | Tratamento de manutenção da doença
pulmonar obstrutiva crónica (DPCO).
Escalão C - 40 %
Calcitriol | pomada | 3µg/g | Silkis® | 30g e 100g |
Lab. Galderma | Tratamento tópico da psoríase em placas,
(psoríase vulgaris), ligeira a moderadamente grave, com um envolvimento
da área de superfície corporal até 35%.
Dutasterida | cápsulas moles | 0,5mg | Avodart® | 10
e 30 unidades | Glaxo Wellcome | Tratamento de sintomas moderados a
graves da hiperplasia benigna da próstata (HBP). Redução
do risco de retenção urinária aguda (RUA) e cirurgia
em doentes com sintomas de HBP moderados a graves.
Escitalopram | comprimidos revestidos | 10mg | Cipralex® |
14 e 28 unidades | H. Lundbeck | Tratamento de episódios depressivos
major. Perturbações de pânico com ou sem agorafobia.
Lutropina alfa | Pó e solvente para solução
injectável | 75 UI/1ml | Luveris® | 1 e 3 unidades (ampola
c/ solvente ou frasco para injectável | Serono Europe | Estimulação
do desenvolvimento folicular em mulheres com insuficiência grave
de LH e FHS, em associação com uma preparação
de FSH.
Metilfenidato | comprimidos de libertação prolongada
| 18mg e 36mg | Concerta® | 30 unidades | Janssen-Cilag | Como
parte de um programa abrangente de tratamento da Perturbação
de Hiperactividade e Deficiências de Atenção (ADHD)
em crianças (maiores de 6 anos) e adolescentes, quando as outras
medidas isoladas para a correcção desta perturbação
se revelam insuficientes.
Pilocarpina | comprimidos revestidos | 5mg | Salagen® | 21
e 84 unidades | Novartis Farma | Alívio dos sintomas de hipofunção
das glândulas salivares em doentes com xerostomia grave após
irradiação da cabeça e do pescoço. Tratamento
dos sintomas de secura da boca e de secura ocular em doentes com síndrome
de Sjogren.
Escalão D - 20 %
Leflunomida | comprimidos revestidos | 10 e 20mg | Arava® |
30 unidades (frasco) | Aventis Pharma | Indicada no tratamento de doentes
adultos com artrite reumatóide activa, como um "medicamento
anti-reumático modificador da doença" (MARMD).
Pioglitazona | comprimidos | 15 mg e 30 mg | Actos® | 28 unidades
| Takeda Europe | Rosiglitazona | comprimidos | 4mg | Avandia®
| 4mg - 7 e 28 unidades | 8mg | 28 unidades | SmithKline Beecham plc |
A pioglitazona e a rosiglitazona estão indicadas em monoterapia
via oral de doentes com diabetes mellitus tipo 2, particularmente em doentes
com excesso de peso, inadequadamente controlados por dieta e exercício
físico, para os quais a metformina é inapropriada devido
a contra-indicações ou intolerância. Estão
também indicadas para terapêutica de combinação
oral em doentes com diabetes mellitus tipo 2, com controlo insuficiente
da glicémia apesar do tratamento em monoterapia oral com a dose
máxima tolerada, quer com metformina, quer com uma sulfonilureia:
- em combinação com metformina particularmente em doentes
com excesso de peso; - em combinação com uma sulfonilureia
apenas em doentes com intolerância ou contra-indicação
para a metformina.
|
|
* Embalagens disponíveis no mercado, conforme informação
do titular de AIM. |
| Consulte
Resumo
das Características do Medicamento (RCM), disponíveis através
do CIMI. |
| Novo
escalão de comparticipação 20% |
| Está
a ser aplicado o novo escalão de comparticipação provisório
de 20% para os medicamentos tenham alguma evidência científica
de mais valia terapêutica ainda que não claramente comprovada.
A situação de comparticipação definitiva depende
da apresentação dos estudos científicos comprovativos. |
| [substâncias
activas ou indicações terapêuticas novas] |
 |
|
Adalimumab
| solução injectável | 40mg/0,8 ml | Humira®
e Trudexa® | 1,2,4 e 6 unidades | Abbott | Tratamento da artrite
reumatóide activa moderada a grave em doentes adultos nos casos
em que foi demonstrada uma resposta inadequada a medicamentos anti-reumáticos
modificadores da doença, incluindo o metotrexato.
Bussulfano | concentrado para solução para perfusão
| 60mg/10 ml | Busilvex® | 8 ampolas | Pierre Fabre | Seguido de
ciclofosfamida (BuCy2) está indicado como tratamento de condicionamento
prévio ao transplante de células progenitoras hematopoiéticas
em doentes adultos em que a associação é considerada
a melhor opção disponível.
Iloprost trometamol | solução para inalação
por nebulização | 10mg/2ml | Ventabis® | 30, 100 e 300
unidades | Schering A.G. | Tratamento de doentes com hipertensão
pulmonar primária, classificada como classe funcional III da NYHA,
para melhorar a capacidade de exercício e os sintomas.
Consulte
Resumo das Características do Medicamento, disponível no
site da EMEA.
|
Zidovudina
Irex
100mg cápsulas duras | 100 unidades
250mg cápsulas duras | 40 e 300 unidades
300mg comprimidos | 60 e 300 unidades |
|
Centro
do Medicamento e dos Produtos de Saúde
Centro de Documentação
Técnica e Científica
O INFARMED dispõe de dois Centros de contacto que prestam apoio
no acesso a informação científica, regulamentar e
estatística na área dos medicamentos, produtos de saúde
e farmácia. Os Centros actuam através do esclarecimento
de questões colocadas pelos profissionais de saúde e pelos
utentes - CIMI - e através da consulta a um fundo documental especializado
nas áreas referidas - CDTC.
À disposição de profissionais de saúde e utentes
está ainda a Linha Verde do Medicamento, através da qual
pode ser prestada qualquer tipo de informação.
|
|
CIMI
2.Ş - 6.Ş | 9h - 18h
E-mail cimi@infarmed.pt
Fax. 21 798 7107
Tel. 21 798 7373
Linha verde - 800 222 444
|
CDTC
2.Ş - 6.Ş | 9h - 18h
E-mail cdtc@infarmed.pt
Fax. 21 798 7107
Tel. 21 798 7171 /5287/7173 |
| Como
receber a Infarmedia ? |
|
Para
sua comodidade, esta informação poderá ser enviada
por e-mail, facilitando ainda consulta imediata da informação
adicional contida nos links.
Inscreva-se em:
www.infarmed.pt/infarmedia
Tel. 21 798 7373 - Fax. 21 798 7107
E-mail: newsinfarmedia@infarmed.pt
A Infarmedia continuará a ser enviada em papel aos profissionais
de saúde que não optem pela inscrição online.
|
|


